前言
过继细胞治疗(ACT)是一种利用患者自身免疫细胞来发现和消除肿瘤细胞的免疫疗法,它利用患者自身(自体移植)或供体(异体移植)的免疫细胞来改善免疫功能。CAR-T目前是研究最热门的领域,然而虽然CAR-T在血液肿瘤获得了巨大的成功,对于实体瘤仍然疗效有限。
肿瘤浸润淋巴细胞(TILs)过继疗法在实体瘤的治疗中展现了强大的疗效,在黑色素瘤、宫颈鳞状细胞癌和胆管癌等多种癌症中引起客观的肿瘤消退,大约25%的患者能够完全治愈,一半以上的患者转移瘤缩小。TIL具有多种TCR克隆性、优越的肿瘤归巢能力和较低的靶向毒性,使其在治疗实体瘤方面具有其他过继性细胞治疗方法无法比拟的优势。尽管如此,TIL治疗的成功应用目前仍局限于几种类型的肿瘤。
下面我们来一起回顾TIL的发展历史和目前临床试验的现状,展望未来的临床应用。
TIL的发展史
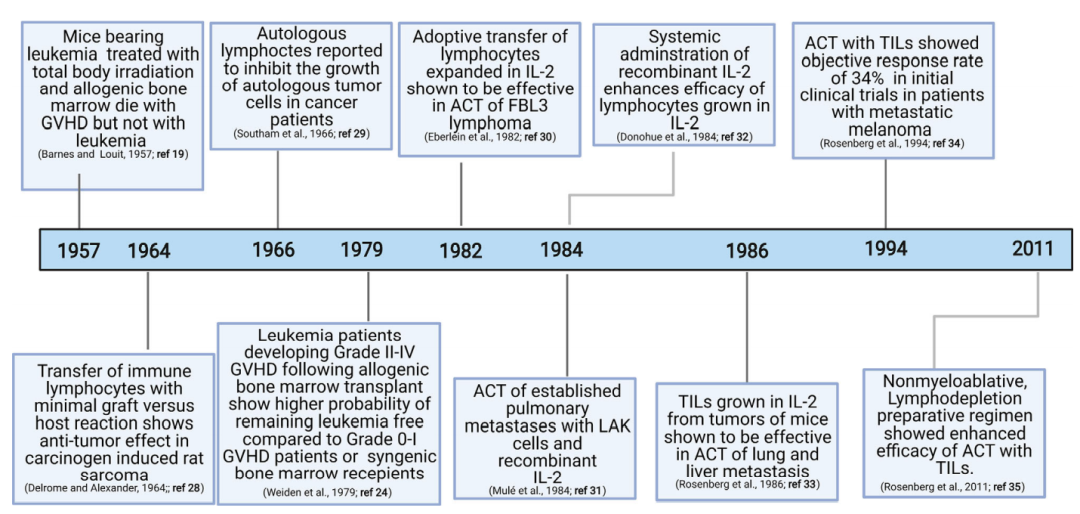
在上世纪50年代,随着移植物抗肿瘤反应的发现以及T细胞在此过程中所起的关键作用,促使人们开始积极探索T细胞在抗肿瘤免疫中的作用。1982年,这一领域的先驱Steven Rosenberg博士和美国国立卫生研究院(NIH)的同事首次从多种小鼠肿瘤模型中分离出TIL,后来证明TIL联合IL-2治愈100%MC38肝转移结肠腺癌小鼠和50%的肺转移小鼠,这为TIL治疗晚期恶性肿瘤的临床应用奠定了基础。TIL在临床上治疗的最早尝试可以追溯到1988年,在转移性黑色素瘤中达到了60%的客观有效率(ORR)。
TIL的产生过程通常始于前快速扩增阶段(pre-REP),在此阶段TIL从肿瘤碎片中分离,并经过初步扩增。然后TIL在快速扩增阶段(REP)中进一步扩增以响应刺激物,例如IL-2和/或饲养细胞。传统的TIL产生是为了特异性的肿瘤识别而进行的,通常需要6-8周。然而,TIL在体外长期培养后容易衰竭,在患者体内不能长期存活。此外,体外培养自体肿瘤的成功率较低,导致接受TIL治疗的患者退出率超过50%,极大地限制了其临床应用。
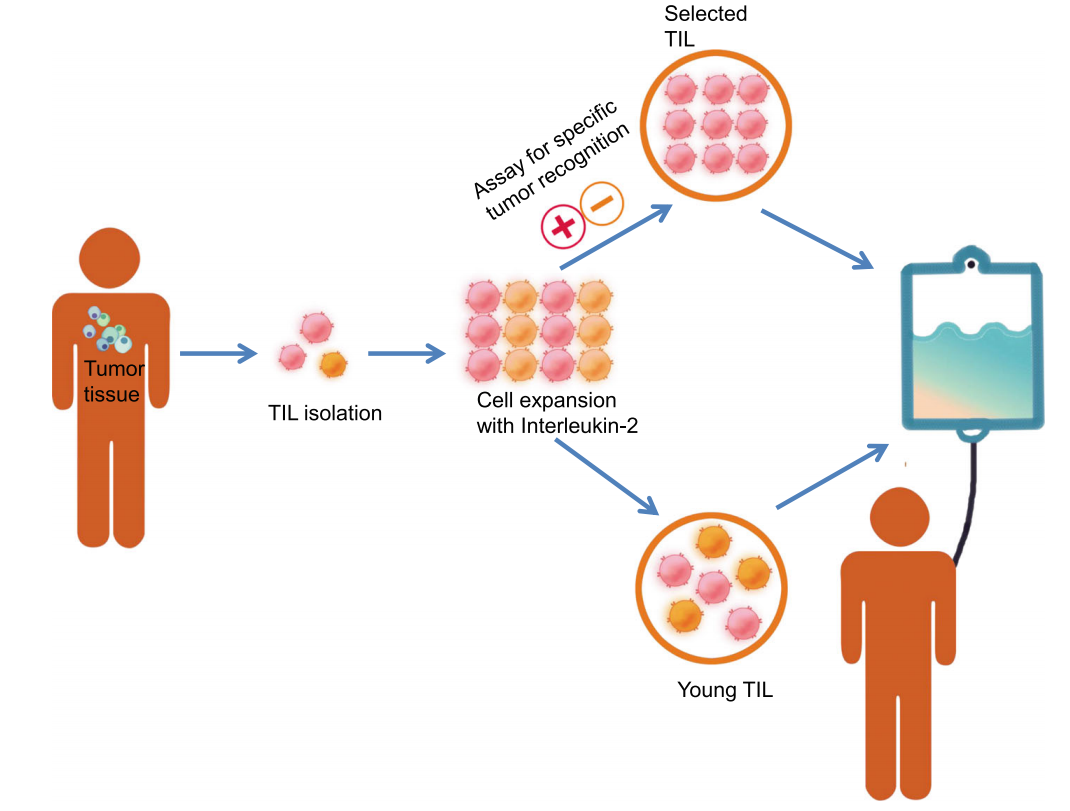
为此,Rosenberg博士等人开发了一种“young TIL”的方法,这种方法可以在没有体外肿瘤反应性选择的情况下快速扩增TIL,从而显著提高TIL产生的时间及其在体内的存活率和疗效。后来,“Young TIL”在黑色素瘤患者中显示出与传统TIL相当的临床结果。
已有研究表明,抗PD-1、抗4-1BB或抗CTLA-4可增加TIL的扩增。与单独使用IL-2相比,IL-2/15/21联合应用可增强肺癌和结直肠癌中TIL的扩增,提高CD8+T细胞百分比和TCR克隆多样性。
TIL的组成和表型选择
最近的研究表明,用于ACT的TIL的组成和表型在决定治疗结果方面起着重要作用。在肿瘤免疫治疗中,除了最多关注的CD8+T细胞,CD4+T细胞也在肿瘤排斥反应中发挥作用。例如,在一名胆管癌患者的TIL中鉴定出MHCII抗原HLA-DQO6限制性CD4+T细胞可以识别ERBB2IP突变。虽然大剂量的TIL使用未能显示任何客观的临床反应,但富集了95%以上ERBB2IP突变反应性CD4+T细胞的TIL诱导了肝和肺转移的显著消退。同样,过继转移产生IL-17的辅助性T细胞(Th17)可诱导持久的抗肿瘤免疫,表明CD4+T细胞的极化在决定抗肿瘤免疫中起着重要作用。总的来说,这些数据表明,囊括CD4+和CD8+T细胞可能是产生有效的TIL-ACT的良好治疗策略。
实际上,只有一小部分TIL(约30%)是肿瘤反应性的。选择肿瘤反应性TIL可显著缩短培养时间,减少输注细胞数。PD-1在黑色素瘤反应性TIL上高表达,PD-1阳性TIL显示出比PD-1阴性TIL更高的肿瘤反应性。此外,用4-1BB筛选的黑色素瘤患者肿瘤反应性TIL,与未选择的TIL相比,显示出增强的肿瘤反应性。
除了包含不同的T细胞亚群外,另一个与TIL持续性相关的因素是干细胞样细胞的存在。最近的一项研究表明,少数具有干细胞样表型的记忆祖细胞CD8+T细胞(CD39-CD69-)是癌症完全消退和TIL持久存在的原因。
TIL治疗实体瘤的特点
实体瘤区别于血液瘤的一些特性给开发有效的过继细胞疗法带来重大挑战。首先,实体瘤的高度异质性使得很难找到针对所有肿瘤细胞的理想靶点,针对单一肿瘤抗原通常导会致抗原丢失或更具攻击性的克隆复发。其次,即使过继转移大量T细胞,大部分实体瘤也很难浸润。还有,肿瘤微环境(TME)存在多种免疫抑制机制,使T细胞的功能很难充分发挥,这些抑制包括但不限于免疫抑制分子、细胞因子和代谢物的上调、共刺激分子的下调以及免疫调节细胞亚群的存在,如Tregs、MDSCs和TAMs。
TIL在治疗实体瘤方面可能有一些独特的优势。首先,TIL由具有多个TCR克隆的T细胞组成,能够识别一系列肿瘤抗原,因此与其它过继性细胞治疗(如CAR-T和TCR-T)相比,TIL在处理肿瘤异质性方面可能更具优势。与此相一致,TIL在含有高突变负荷的实体瘤(如黑色素瘤)中显示出比CAR-T更好的临床疗效。其次,在体内受肿瘤抗原刺激后,TIL往往主要由效应记忆T细胞(Tem)组成,其表面表达趋化因子受体,如CCR5和CXCR3。与肿瘤特异性TCR一起,TIL在转移到患者体内后,可以很容易地定位于表达抗原的组织,包括肿瘤。最后,在TIL治疗中很少报道靶向毒性,这可能是由于在T细胞免疫的早期发展过程中,TIL的TCR阴性选择所致。
TIL的临床研究进展
迄今为止,已经完成了许多TIL-ACT的临床研究,其中一些研究显示了令人鼓舞的结果。Iovance Biotherapeutics开发的商用自体TIL产品lifileucel(LN-145、LN-144和LN-145-S1)正处于II期临床开发阶段,用于治疗不能切除或转移的黑色素瘤、复发或转移的头颈部鳞状细胞癌(HNSCC)、复发或转移的非小细胞肺癌(NSCLC)。其中LN-145在27例至少接受过一次化疗的晚期宫颈癌患者中显示出了良好的初步疗,观察到44%的客观响应率,包括1个CR和9个PR。FDA已经授予LN-145突破性疗法,用于治疗复发性、转移性或持续性宫颈癌以及化疗前后的疾病进展。
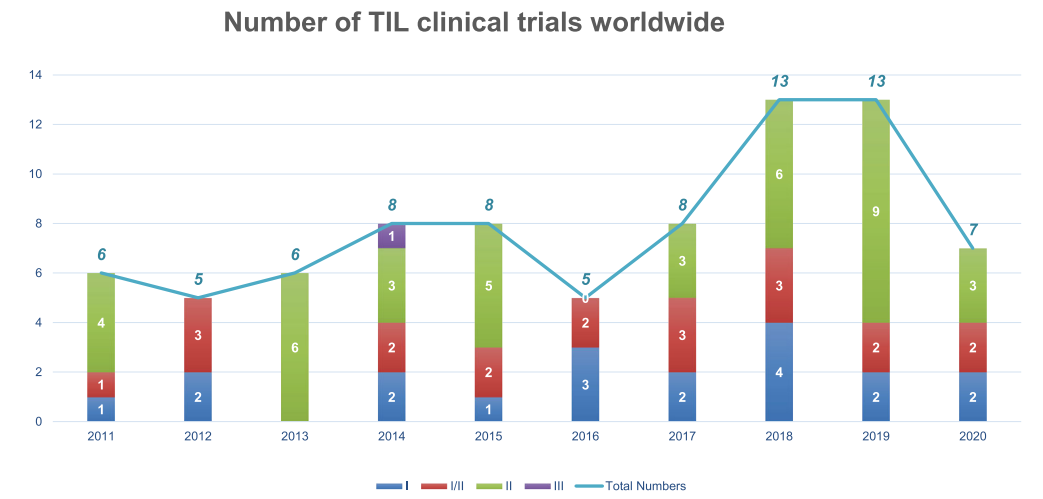
在2011年至2020年间,共有79项TIL治疗的临床试验,包括22种TIL产品。试验数量在2018年和2019年达到峰值。
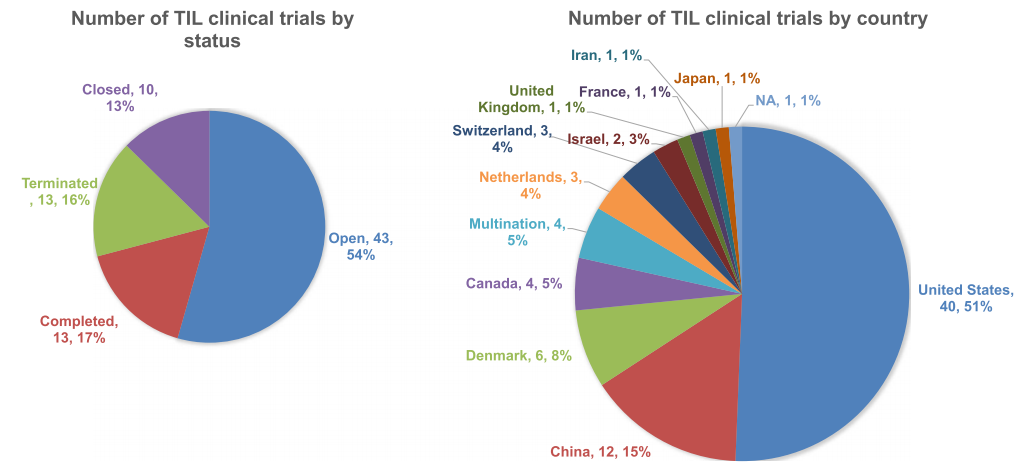
目前,54%(43/79)的试验正在进行,17%(13/79)的试验已经完成,其余的试验要么已经结束,要么已经终止。区域分析显示,这些试验中有51%(40/79)在美国进行,15%(12/79)在中国进行。
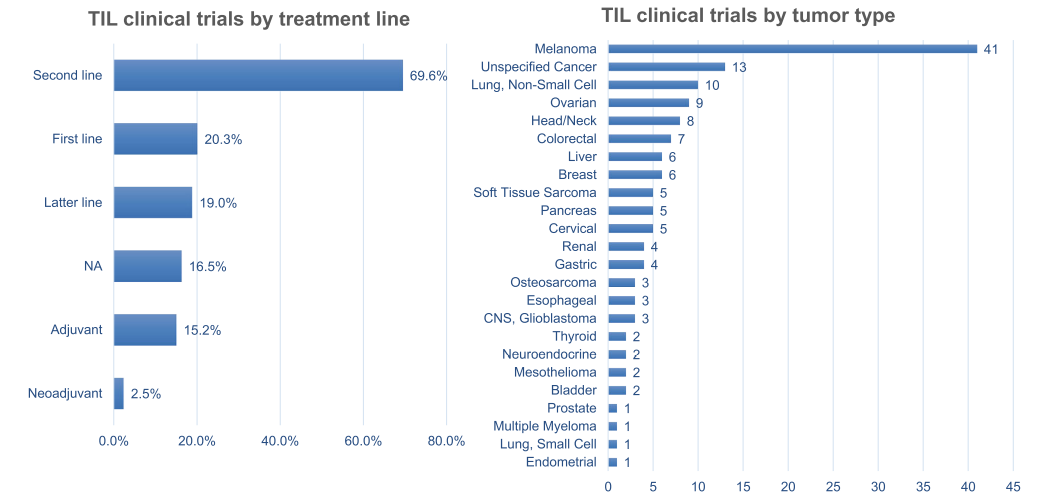
TIL疗法目前主要作为二线治疗进行临床试验。在大多数临床试验中,黑色素瘤仍然是头号肿瘤类型,其次是NSCLC、卵巢癌和头颈癌。到目前为止,TIL治疗在转移性黑色素瘤和晚期宫颈癌中已经显示出令人印象深刻的临床益处,甚至在使用检查点抑制剂治疗的患者中也是如此。NSCLC、结直肠癌(CRC)和乳腺癌也证明了初步疗效。
然而,高剂量的IL-2作为支持输注的TIL生长和活性的常规使用,可能会限制TIL治疗的临床应用。高剂量的IL-2通常会引起全身毒性,需要加强监测和护理,还可能促进抑制TIL抗肿瘤反应的调节性T细胞。尽管在低剂量或中剂量IL-2的试验中可以达到30%以上的ORR,但大多数TIL试验仍然采用高剂量IL-2输注。此外,不可持续的体内存活和TME中的免疫抑制也是实现TIL治疗最大的障碍。
尽管如此,TIL疗法依然展现出其强大的肿瘤杀伤效果。截至2021年3月12日,有许多TIL -ACT临床研究招募患者,包括胆道癌(NCT03801083)、转移性葡萄膜黑色素瘤(NCT03467516)、妇科肿瘤(NCT04766320)、预处理转移性三阴性乳腺癌(NCT04111510)、非小细胞肺癌(NCT04614103)的试验,结直肠癌(NCT03904537)、卵巢癌(NCT04072263)、宫颈癌(NCT04443296)、复发或难治性卵巢癌、间变性甲状腺癌、骨肉瘤或其他骨和软组织肉瘤(NCT03449108)等。
新一代的TIL
为了降低大剂量IL-2的毒性,提高传统TIL治疗的体内存活率和功能,新一代TIL产品正在积极研究中。新一代TIL是一种转基因TIL,通过病毒转导过度表达一个感兴趣的基因,或 者通过CRISPR或TALEN等技术敲除(KO)目标基因。
然而,新一代TIL的发展可能面临一些重大挑战。基因编辑在TIL中可能在技术上很难实现,这是由于TIL的多种细胞组成以及不同的生长速率。此外,在TIL中选择合适的靶向基因也是一个关键而具有挑战性的问题。
到目前为止,新一代TIL在临床上的尝试主要集中在工程化TIL以过度表达细胞因子,如IL-2和IL-12。在一项I/II期试验中,IL-2插入TIL后在体外显示出存活率的提高,但在体内的持久性和临床疗效几乎没有改善。另一个I期试验使用了NFAT诱导表达的IL-12工程化TIL,在转移性黑色素瘤显示出良好的临床疗效,使用比传统TIL治疗少10-100倍的细胞数量,获得了63%的ORR,但是血清中IL-12和IFN-γ水平异常升高,且毒性显著。
因此,新一代的TIL在进入临床之前,需要对转基因TIL进行全面的安全性和功能评价。除了体外鉴定外,还需要建立动物模型来更好地了解修饰TIL在体内的持久性、功能以及毒性。
小结
TIL-ACT是一种很有前途的新兴实体瘤免疫治疗方法,有望在不久的将来应用于临床。TIL-ACT有不可否认的优点:a)强有力的、可重复的临床反应;b)有能力使经过多次治疗的晚期肿瘤患者受益,这些患者已经没有其他治疗选择。
然而,与这些疗法的生产和提供有关的挑战有很多。因为必须为每个患者生产特定的产品,这需要高度专业化的良好生产规范(GMP)设施和训练有素的员工,导致成本高昂。此外,生产过程需要时间,通常超过一个月,这对肿瘤进展迅速的患者来说可能太长。
这种治疗方法还有很大的改进空间和更广泛的应用,包括与免疫检查点抑制剂的联合应用,联合溶瘤病毒也在探索中。尽管TIL疗法在我国尚处于起步阶段,国内整体行业的蓬勃发展营造了良好的宏观环境,相信在各方的合作和共同努力下,TIL疗法很快会使更多的实体肿瘤患者中收益。